
S'anomena vapor una substància a la fase de gas que es troba a una temperatura més baixa que el punt crític. A causa d'aquesta característica, el vapor es pot condensar en un líquid o sòlid incrementant-ne la pressió sense reduir la temperatura.
És a dir, és un gas que es pot condensar a temperatura constant augmentant-ne la pressió. D'altra banda, per convertir un gas no vaporós a líquid, no n'hi ha prou a augmentar la pressió, sinó que caldrà disminuir la temperatura.
Per exemple, l'aigua té una temperatura crítica de 374°C (647 kelvin), la qual és la temperatura més alta en què hi pot haver aigua líquida.
El vapor pot coexistir amb líquid o sòlid. En aquest cas, les dues fases estaran en equilibri i la pressió de gas serà igual a l'equilibri pressió de vapor del líquid (o sòlid).
Normalment, la paraula vapor, si no s'especifica de quina substància es tracta, se sol referir al vapor d'aigua.
Què és el vapor daigua?
El vapor d'aigua és un gas que es produeix per ebullició quan l'aigua s'escalfa a 100°C (punt d'ebullició de l'aigua) i una atmosfera de pressió.
En aquest punt es diu que laigua està en un canvi de fase. En aquest instant si seguim subministrant calor no augmenta la temperatura fins que no s'hagi evaporat l'aigua.
En aquestes condicions de pressió, per sobre dels 100 graus Celsius, l'aigua pura es troba en estat gas.
Sovint utilitzem aquest terme per referir-nos al vapor humit, l'aerosol de les gotes d'aigua que es formen en condensar-se, boira, etc. Tot i això, el vapor sec és invisible.
La humitat relativa és la relació entre la pressió parcial del vapor d‟aigua en un gas (principalment al‟aire) i la pressió d‟equilibri del vapor saturat a una temperatura donada.
La humitat absoluta és la quantitat de vapor daigua que conté 1 metre cúbic daire a una temperatura determinada.
Què significa estat de vapor?
L'estat de vapor és l'estat en què hi ha un gas quan es troba per sota de la temperatura crítica.
A l'estat gas les molècules que la formen no reaccionen entre si formant enllaços moleculars, sinó que tendeixen a repel·lir-se mútuament. Quan es repel·leixen, les molècules d'aigua adopten la forma i el volum del recipient que les conté i tendeixen a separar-se i ocupar tot el volum disponible.
Quina diferència hi ha entre gas i vapor?
El vapor és un tipus de gas però no tots els gasos són vapor.
Si comprimim un gas mantenint la temperatura, el gas no canvia d'estat, encara és gas. En canvi, en augmentar la pressió a temperatura constant, al vapor sí que es pot tornar líquid.
El gas ocupa tots l'espai disponible mentre que el vapor no es comporta així.
Quina importància té el vapor?
Aquest element és essencial per al desenvolupament de la vida a la Terra per les seves propietats i la seva presència a l'atmosfera. A més, l'ésser humà ha estat capaç d'aprofitar-lo per obtenir una feina mecànica i produir electricitat.
Importància al medi ambient
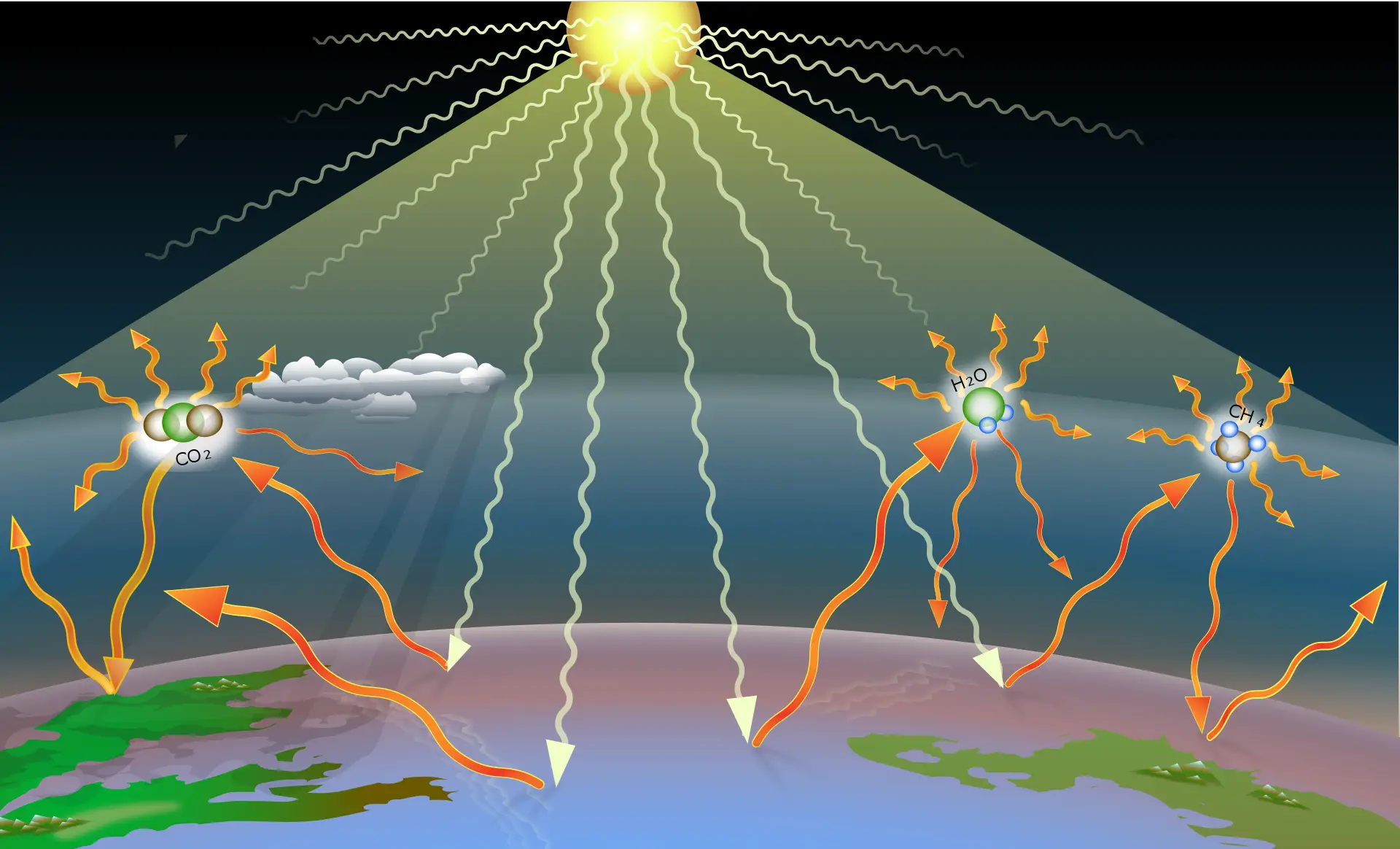
El vapor daigua a latmosfera és un gas defecte hivernacle igual que ho és el diòxid de carboni. Parteix de la radiació solar que entra a l'atmosfera, rebota contra la superfície de la Terra i surt de nou a l'exterior. Tot i això, els gasos hivernacle retenen aquesta calor contribuint a l'escalfament global.
El vapor d‟aigua atmosfèric és part del cicle hidrològic, un sistema tancat de circulació d‟aigua des dels oceans i continents al‟atmosfera i viceversa, en un cicle continu d‟evaporació, transpiració, condensació i precipitació.
Importancia en la indústria
Les propietats del vapor van permetre desenvolupar la màquina de vapor que es va utilitzar àmpliament durant la revolució industrial.
Aquest tipus de màquines s'utilitzaven per accionar màquines però també per al transport, com per exemple a les locomotores de vapor.
Generació elèctrica
El vapor també s'utilitza a les centrals tèrmiques per generar electricitat.
Tant les centrals tèrmiques convencionals com les centrals nuclears utilitzen l'energia tèrmica que obtenen de les fonts de calor (combustibles fòssils i energia nuclear) per generar vapor a alta pressió i accionar turbines de vapor.
Les turbines estan connectades a un generador elèctric que converteix lenergia mecànica en energia elèctrica.


